2018-04-13
引言:
自2012年宾大Carl June教授采用CD19-CAR-T细胞成功治愈一位晚期B细胞白血病小女孩Emily后,CAR-T治疗便在医学界声名鹊起;2017年FDA相继批准诺华和吉利德的CD19-CAR-T细胞新药(Kymriah和Yescarta)上市,更是催生更多的社会资源往这一领域倾斜。然而,天价的产品却让很多患者望而却步!就在近日,美国医保CMS居然放大招:将有效患者的CAR-T治疗纳入医保,同意为特定肿瘤患者支付数十万美元用于CAR-T治疗[1]!这一举措无疑会大大推动CAR-T细胞的临床应用。随着CMS打开了为患者CAR-T治疗承担费用的大门,这似乎意味着会有更多的国家会将此项治疗纳入医保范围。
面对当前如火如荼的细胞治疗研发和商业化进程,人们不禁会问:“活细胞”是否适合作为一种稳定的药物形式?细胞治疗能否发展成为一种成熟的制药产业?本文从以下几个方面进行阐述,分享个人对CAR-T细胞治疗发展的几点看法——CAR-T治疗正在引领细胞药物时代的到来。

近日的Emily(CAR-T治疗后康复5年)
1、颠覆性的疗效
疗效是检验一项治疗技术或创新药物是否具有强大生命力的金标准。CAR-T细胞治疗率先在血液肿瘤治疗上展现了全面优于传统治疗的颠覆性疗效[2]。如下为在2017年底在美国血液学年会(ASH)汇报的最新结果:
l Novartis:一项名为JULIET的临床试验数据显示:6个月内,81例接受Kymriah(即CTL019)治疗的复发或难治性弥漫性大B细胞淋巴瘤患者达到持续缓解。ORR为53%,CR为40%,PR为14%。6个月后,ORR为37%,CR为30%;
l Kite:一项名为ZUMA-1临床研究的长期、随访性数据显示:难治性大B细胞淋巴瘤患者在进行单次静脉滴注Yescarta(即KTE-019)1年后(中位随访时间15.4个月),42%的患者达到持续缓解,其中CR为40%;
l Juno:一项名为TRANSCEND的临床试验数据显示:接受JCAR017治疗的复发难治性非霍奇金淋巴瘤患者中,3个月内ORR为74%,CR为68%,6个月内CR为50%,同时显示出比Kymriah和Yescarta更好的安全性;
l Bluebird and Celgene:一项名为CRB-401临床研究数据同样令人惊艳:18例接受高剂量(≥150*106)bb2121(anti-BCMA-CAR-T)治疗的复发难治性多发性骨髓瘤患者中,94%产生应答,PR为89%,CR为56%,6个月和8个月DFS分别为81%和71%。
l 值得骄傲的是国内CAR-T研发企业展现了毫不逊色于国际巨头的临床数据,在有些癌症治疗方面,国内的CAR-T治疗效果还要更优于外国。
注:上述术语缩写注释:

2、明确的作用机制
明确的药效作用机制,是创新药物能够被临床接受和推广的重要前提。随着基础医学特别是免疫学的发展,人们对肿瘤与免疫的理解逐渐深入。作为抗肿瘤免疫中最重要的成员T细胞,在接受抗原提呈细胞提供的双信号后开始活化、增殖,一方面分泌颗粒酶、穿孔素直接裂解癌细胞,另一方面通过Fas-FasL信号通路诱导癌细胞凋亡。CAR技术是通过基因工程手段将T细胞活化的双信号嵌合成一个分子,表达在T细胞膜上,可突破MHC限制。当CAR-T细胞识别癌细胞上的靶点后,快速活化、增殖,展现强大的抗肿瘤功能。
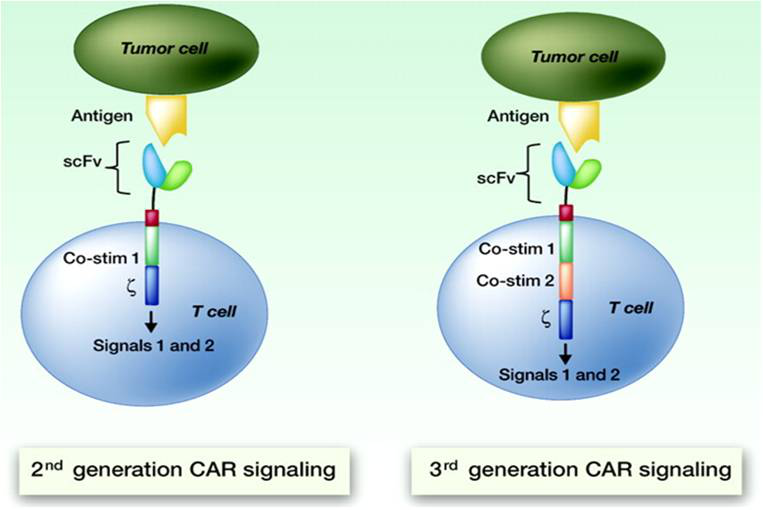
CAR-T杀伤肿瘤细胞的作用机制
3、日趋完善的生产工艺和质控标准
活细胞作为一种新型药物载体,尚未形成像化学小分子和生物大分子那样成熟、标准化的生产工艺和统一的质控标准,这是制约细胞药物能否发展成为成熟产业的关键因素。2018年3月13日,CFDA药品评审中心(CDE)及时颁布了CAR-T细胞IND指导原则,对生产工艺和质量控制提出了几点建议[3]。
生产工艺中的试剂、培养基、质粒、病毒等质控标准容易达成行业共识,但目前的CAR-T治疗属于个性化治疗,细胞提取自患者自身,原料细胞及制备的CAR-T细胞质控参数差异较大,其质控标准难以达成共识。这迫切需要发展一种通用型CAR-T细胞技术,尽可能在同一批次的原材料和终产品的质控参数上实现稳定,适应药物的生产和质控标准。
国际上Cellectis利用TALEN基因编辑技术生产的UCART-19已在进行临床试验,成功治愈一位1岁白血病儿童;国内邦耀生物公司也正在利用基因编辑技术开发的UCART(通用性CART)已完成研发生产工艺验证,正在启动与中南大学湘雅医院的临床试验研究并进行IND申报。
随着基因编辑技术的进步及在细胞治疗领域的应用,源自健康人T细胞的通用型CAR-T成为发展趋势,其生产工艺和质控标准将会日趋完善,形成行业共识,推动CAR-T细胞坚定不移地走向细胞药物的道路。
4、丰富的临床治疗经验和科学的疗效评估体系
目前,美国Clinical trials网站注册的CAR-T临床试验数目多达300余项,全球顶尖的癌症治疗医院均参与到CAR-T临床试验中,从化疗药物的预处理、CAR-T细胞剂量的设计、适应症的选择、副反应的处理到与其他疗法的连用,都积累了丰富的治疗经验。以前谈之色变的细胞因子风暴得到了很好的管控;脱靶效应、神经毒性等副反应的原因也渐清晰,并可对症处理。CAR-T细胞治疗正在建立一套成熟的可推广的临床治疗体系。
与此同时,美国Memorial Sloan-Kettering癌症中心Wolchok教授在Clinical Cancer Research撰文发表了适合免疫治疗的临床疗效评估标准,弥补了RECIST (response evaluation criteria in solid tumor)或改良后的WHO标准并不完全适用于抗肿瘤细胞免疫治疗的缺陷[4]。如下表为:新的免疫治疗疗效评价标准( immune-related response criteria,irRC)和WHO的比较:
在免疫治疗实践中发现肿瘤患者出现新的病灶并不一定提示治疗无效,相当比例的患者继续接受治疗,出现SD,PR甚至CR。多数免疫治疗起效缓慢,短期内出现新病灶或瘤负荷量稍增加并不一定是恶化表现;更为重要的是免疫细胞攻击肿瘤细胞,导致肿瘤细胞大量坏死,故导致肿瘤组织水肿,通常会使瘤体积增大,易导致疾病恶化的误判。

irRC 与传统WHO 标准的比较[4]
5、成型的商业模式
如同生产关系一定要适应生产力的发展,CAR-T细胞作为刚刚兴起的药物,能否形成与之配套的商业模式很大程度上制约了CAR-T细胞药物的临床应用,也决定了细胞治疗最终能否发展成为一种成熟的制药产业。随着资本的疯狂涌入,优秀的CAR-T研发企业一般不差钱,临床试验取得较好数据后的再融资或商业授权更是可以为企业获取源源不断的现金流,支撑企业的发展;生产基地的同质化管理,专业化的冷链物流配送保障了CAR-T细胞保质生产和安全运输;和老牌医药公司的合作有利于CAR-T细胞的市场开发和商业销售。
近日,美国诺华公司推出的按疗效付费的支付方式和美国政府将CAR-T细胞纳入医保的决策更是打通了CAR-T细胞商业化的最后一公里,2018年CD19-CAR-T在美国的销售额必将大幅增长,这也预示着有更多的国家(如中国)会将此项治疗纳入医保范围。综上,CAR-T细胞的商业模式基本成型,产业资本+研发企业+老牌医药公司这样的联合体可以构建资本+产品+销售这样相对完善的商业模式。
可以预见,CAR-T细胞作为癌症治疗的突破性疗法,在各国政策的扶持下,在庞大的人才红利下,加上细胞载体本身的高度可塑性,特别是基因编辑技术与细胞治疗结合的产物UCART(通用性CART)的发展,有望更快速、高效实现“现成(off the shelf)”的同批次同质量规模化的细胞药物,这将更快推动细胞治疗药物的产业化之路。
参考资料:
1、Patients receiving FDA-approved CAR-T therapies face potentially prohibitive co-payments.
Apr. 5, 2018 5:39 PM ET|By: Douglas W. House, SA News Editor
责编:黄安玲

中国肿瘤生物治疗杂志 Chin J Cancer Biother. Aug. 2011,